醫療器械軟件臨床試驗服務是道和思源聯合國內醫療器械軟件臨床試驗頂尖專家以及知名醫院重點打造的核心業務之一。醫用軟件臨床試驗是部分二三類醫療器械軟件注冊流程中最為關鍵的一環,它需要得到專業知識、龐大資金以及充足時間來支持。道和思源擁有頂尖的醫用軟件臨床試驗專家,擁有各類醫療器械軟件產品多年臨床試驗服務經驗,具備完善的醫療器械軟件臨床全過程管理能力,以及嚴謹的項目評估能力,為您提供高效率、降成本、保質...
醫療器械軟件臨床試驗服務是道和思源聯合國內醫療器械軟件臨床試驗**專家以及知名醫院重點打造的核心業務之一。醫用軟件臨床試驗是部分二三類醫療器械軟件注冊流程中最為關鍵的一環,它需要得到專業知識、龐大資金以及充足時間來支持。道和思源擁有**的醫用軟件臨床試驗專家,擁有各類醫療器械軟件產品多年臨床試驗服務經驗,具備完善的醫療器械軟件臨床全過程管理能力,以及嚴謹的項目評估能力,為您提供高效率、降成本、保質量的醫療器械軟件臨床試驗服務。
(1)項目可行性調研; (2)倫理遞交;
(3)研究者會議組織; (4)受試者招募;
(5)研究中心信息收集; (6)試驗預算管理;
(7)研究相關培訓; (8)內部稽查;
(9)臨床試驗項目管理; (10)試驗物資和試驗文件管理。
(1)臨床試驗管理; (2)專業臨床研究協調員(CRC)配備;
(3)研究文檔的管理; (4)受試者招募與管理;
(5)研究物資管理; (6)數據管理;
(7)倫理和機構的溝通; (8)安全信息的管理;
(9)研究中心管理; (10)研究中心SOP的建立和完善;
(11)機構認證輔導; (12)研究者及其他參與人員的培訓;
(13)協助機構對在研項目的稽查; (14)協助接受SFDA現場核查;
(15)費用協商。
1.預期的受益應當大于可能出現的損害。
2.完成醫療器械臨床前研究。
3.準備充足的試驗用醫療器械。
4.醫療器械臨床試驗應當在兩個或兩個以上醫療器械臨床試驗機構中進行。
5.申辦者與臨床試驗機構和研究者達成書面協議。
6.列入需進行臨床試驗審批的第三類醫療器械目錄產品的臨床試驗需獲得批準。
7.申辦者應向所在省、自治區、直轄市食品藥品監督管理部門備案。
臨床試驗方案包括:
1. 一般信息
2. 臨床試驗的背景資料
3. 試驗目的
4. 試驗設計
5. 安全性評價方法
6. 有效性評價方法
倫理委員會意見
臨床試驗方案
臨床試驗報告
具體內容詳見《醫療器械臨床評價技術指導原則》
1. 臨床試驗審批定義
對人體具有較高風險的第三類醫療器械進行臨床試驗應獲得國務院藥品監督管理部門批準。
2. 需進行臨床試驗審批的第三類醫療器械目錄
國家藥監局關于發布需進行臨床試驗審批的第三類醫療器械目錄(2020年修訂版)的通告(2020年第61號)
3. 臨床試驗審批流程

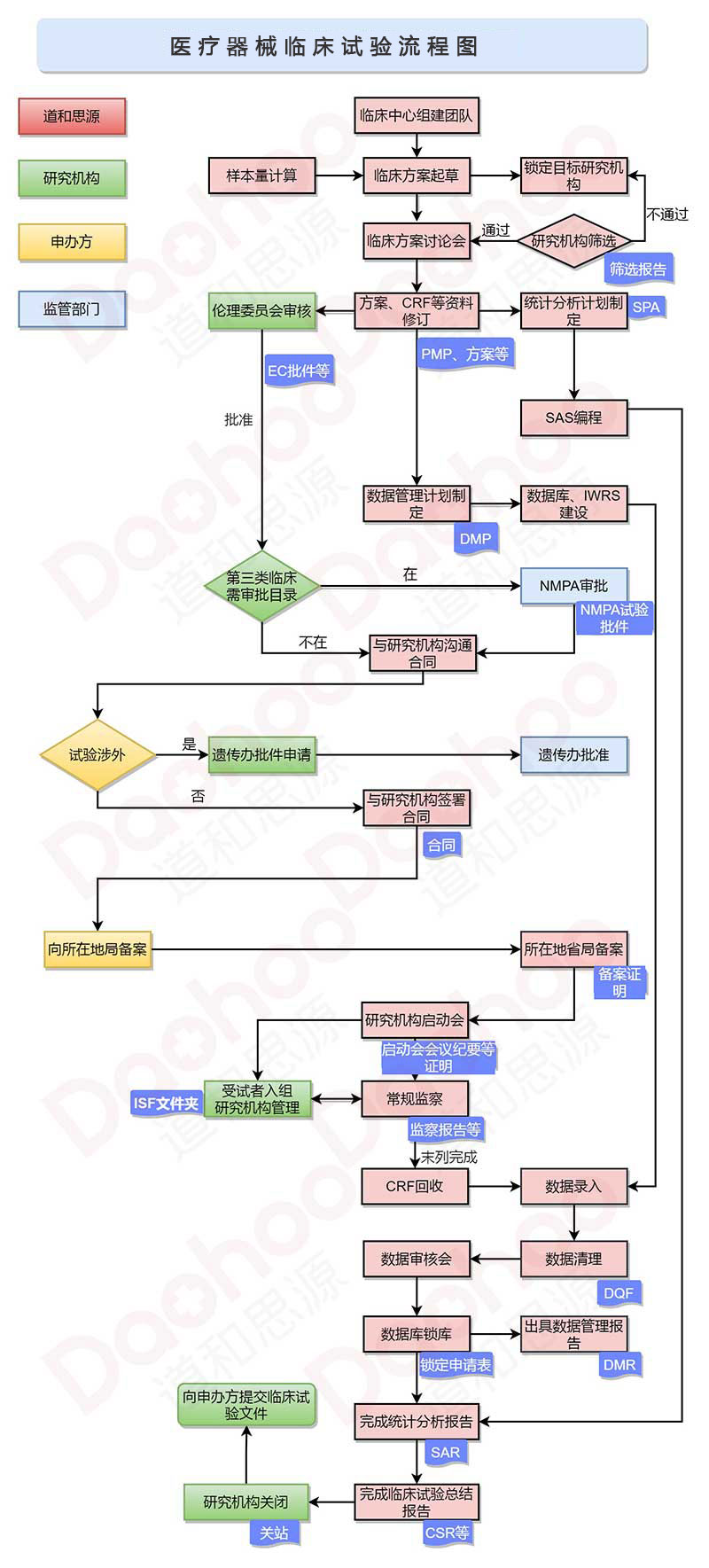
該費用根據產品具體情況來報價,如需產品報價,可直接聯系李經理13521090701
臨床時間是根據產品具體情況來規劃時間的,如需臨床試驗時間,可直接聯系李經理13521090701